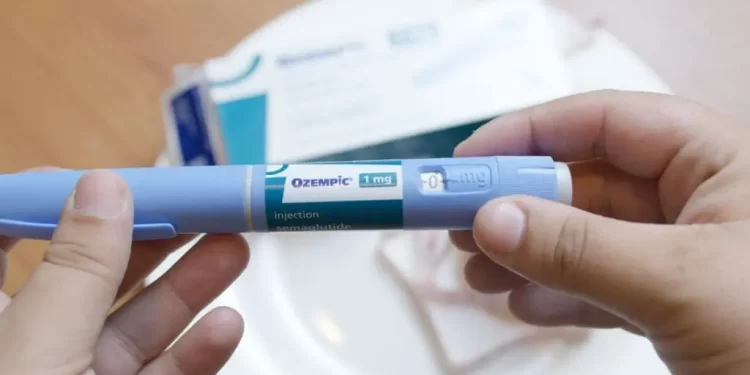
A patente da semaglutida, princípio ativo de medicamentos indicados para tratamentos de diabetes e obesidade, como o Ozempic, termina nesta sexta-feira (20).
Ou seja, a partir desta data, os medicamentos genéricos e similares à base dessa substância poderão ser vendidos no Brasil depois de uma aprovação da Anvisa (Agência Nacional de Vigilância Sanitária).
A expectativa é que a produção dos genéricos torne as canetas emagrecedoras à base de semaglutida — há muitas, todavia, que são à base de tirzepatida — mais baratas e acessíveis aos pacientes. Porém, essa mudança ainda deve demorar até chegar às farmácias.
A quebra da patente poderá desencadear disputas judiciais e desafios regulatórios que podem adiar a entrada efetiva de marcas concorrentes no mercado farmacêutico.
“A quebra da patente é o primeiro passo para que o mercado receba outros produtos de outras marcas […]. Os laboratórios precisarão aprovar as novas substâncias, têm que passar pela Anvisa, passar por um controle de qualidade, para aí sim receber a chancela de distribuição e comercialização”, explicou o especialista em direito médico Murilo Aranha, em entrevista ao News das 19 Horas.
O especialista ainda explicou que a Anvisa tem se prolongado para fornecer as aprovações necessárias e, devido a isso, o governo brasileiro tem gerado uma lista prioritária.
“Por conta de todas as notícias, todos os fatos e casos que tivemos ao longo dos anos em relação a essa medicação sendo usada de forma indevida por laboratórios clandestinos, […] a Anvisa tem sido muito rígida sobre as licenças, e, na prática, ainda não é 100% de certeza que todos os laboratórios estão aptos a utilizar essa substância”, argumentou o especialista.